Science Advances | 单原子纳米酶
大家好,今天分享一篇发表在Science Advances上的文章“Single-atom nanozymes”。本文的通讯作者是来自长春应用化学研究所电分析化学国家重点实验室的董绍俊院士,她的课题组主要研究方向为功能界面电化学,纳米材料,生物电化学和传感器。
纳米酶是一类既有纳米材料的独特性能,又有催化功能的模拟酶。作为一种新型的强催化活性且稳定的天然酶替代物,纳米材料的类酶催化活性在近十几年来引起了人们的广泛关注。尽管经过十几年的发展,纳米酶研究取得了快速的进步,但目前仍面临着两个技术挑战:首先是活性位点密度低的类酶活性纳米酶的催化活性往往远低于天然酶;其次,不同的纳米酶的元素组成和微结构上的差异导致其催化机制的不同,这使得确定实际活性中心和寻找类酶活性的来源变得极为困难。
为了解决这些问题,文章作者提出了一类新型单原子纳米酶,采用将单原子技术与纳米酶的类酶活性中心特性相结合的方式,利用先进的单原子技术进行固有类酶活性位点的设计,发现了原子分散的金属中心使新型纳米酶结构中活性位点的效率和密度最大化。
文章中提出了一种通过模拟酶活性中心空间结构来合成高活性单原子纳米酶的方法。首先设计一种由MOF(金属有机框架材料)包裹的酞菁铁(FePc)(酞菁是一类大环化合物,环内有一个空腔,中心腔内的两个氢原子可以被70多种元素取代,包括几乎所有的金属元素和一部分非金属元素)的主客体结构,然后在900℃的N2气氛下对其进行热解。采用自下而上的方法制备了碳纳米管约束的轴向N原子配位Fe原子的 (FeN5 SA/CNF)纳米酶。
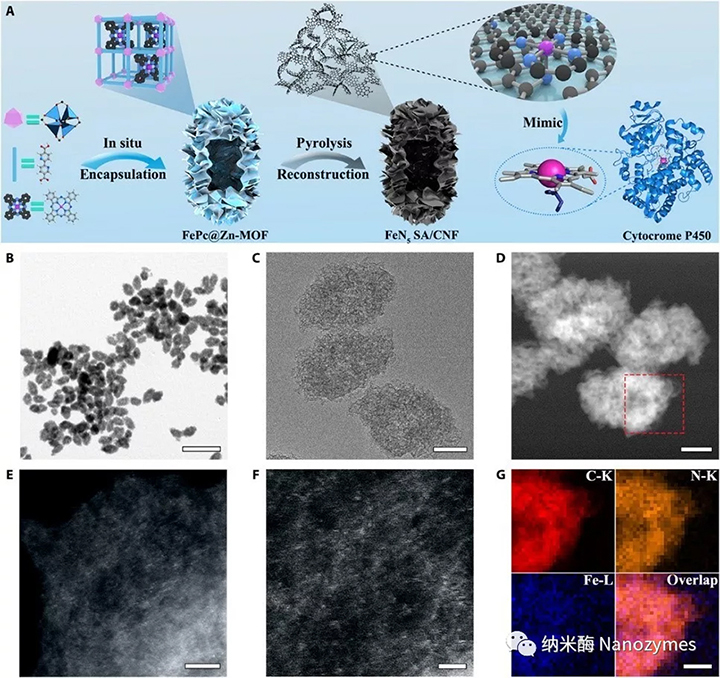
图1 FeN5 SA/CNF的合成方案和形态表征
然后作者以氧化酶催化作为反应模型,通过实验研究和理论计算表明,FeN5 SA/CNF的最主要类氧化酶活性来源于协同效应和电子推动机制。FeN5 SA/CNF活性分别是平面FeN4催化剂和工业铂碳催化剂活性的17和70倍,这表明FeN5 SA/CNF的轴向N原子配位结构具有提高催化活动的作用,增加了对单原子纳米酶的机理理解。
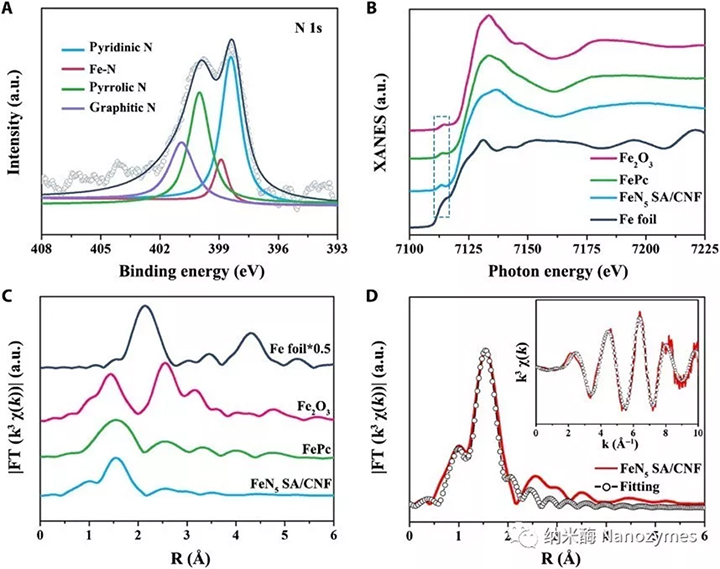
图2 FeN5SA/CNF的原子结构表征
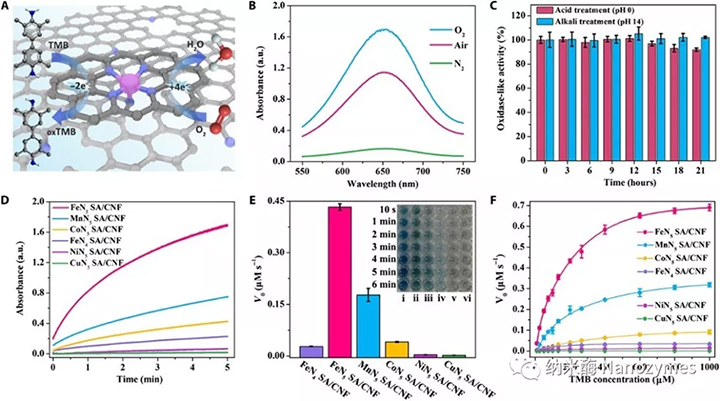
图3 FeN5 SA/CNF的氧化酶样活性
同时,通过体外抗菌实验发现FeN5 SA/CNF在体外表现出较好的杀菌特性,由扫描电镜图像检测出细菌受到严重破坏,细胞形态丢失,出现大面积膜损伤。而通过采用大肠杆菌的伤口感染模型对小鼠进行体内抗菌实验测得FeN5 SA/CNF在体内也表现出良好的伤口消毒效果,在伤口感染和治疗后4天的观察中,与对照组相比,FeN5 SA/CNF组小鼠溃疡明显缓解,伤口愈合速度加快。
总之,文章中提出的单原子纳米酶制造和评价方法为纳米酶的催化机理和合理设计提供了一个新的视角,具有成为新一代纳米酶的巨大潜力。
原文:Single-atomnanozymes
Liang Huang, Jinxing Chen, Linfeng Gan, Jin Wang*and Shaojun Dong*
Science Advances 03 May 2019:
Vol. 5, no. 5, eaav5490
DOI: 10.1126/sciadv.aav5490
原文链接:
https://doi.org/10.1126/sciadv.aav5490
文|刘淑杰、徐风梧
审阅|姜晓倩
编辑|徐庚辰
(本文转载自纳米酶 Nanozymes微信公众号,原文链接:https://mp.weixin.qq.com/s/N6QAQV939ySUOqD192Q_bg)


